研究
筋萎縮性側索硬化症(ALS)を対象とした肝細胞増殖因子(HGF)の第Ⅱ相試験(医師主導治験)を開始
東北大学大学院医学系研究科神経内科学分野の青木正志教授(東北大学病院神経内科 科長)は、大阪大学大学院医学系研究科神経内科学の望月秀樹教授(大阪大学医学部附属病院神経内科・脳卒中科長)と共同で、筋萎縮性側索硬化症(ALS)(※1)患者を対象とする肝細胞増殖因子(HGF)(※2)組換えタンパク質の第II相試験(医師主導治験)(以下、本治験)を実施します。本治験は、日本医療研究開発機構(AMED)の難治性疾患実用化研究事業による支援を受け、東北大学病院および大阪大学医学部附属病院において行います。
ALSは、主に運動神経の変性によって全身の筋肉にやせと筋力低下が進行し、やがては呼吸筋まひにいたる難治性の神経疾患です。症状を改善するような治療法がないため、新しい治療法の開発が切望されています。青木教授を中心とする研究グループはこれまで、日本で発見された神経栄養因子であるHGFを用いたALS治療法の開発に取り組んできました。
HGFはもともと肝細胞の増殖因子として発見された生理活性物質ですが、運動神経細胞の保護効果を示す神経栄養因子としての作用も強く、難治性神経疾患に対する治療薬として臨床応用が期待されてきました。青木正志教授らは、慶應義塾大学医学部生理学教室の岡野栄之教授および整形外科学教室の中村雅也教授、旭川医科大学脳機能医工学研究センターの船越洋准教授らと協同して組換えHGFタンパク質を医薬品化する創薬研究を行い、2011年~2014年、世界初の組換えHGFタンパク質の脊髄腔内投与による第I相試験を東北大学病院で実施しました。その結果、安全性と薬物動態を15名の軽症ALS患者で確認できました。
この成果を経て、今回はALSに対するHGFの有効性と安全性を確認するための第II相試験を計画しました。本治験では、東北大学病院、大阪大学医学部附属病院のそれぞれで24例ずつ、合計48例のALS患者に参加いただく予定です。本治験で使用する治験薬は、ヒトのHGFを遺伝子組換え技術により製造・製剤化したもの(開発コード:KP-100IT)で、クリングルファーマ株式会社から提供されます。
本治験の実施については、東北大学病院および大阪大学医学部附属病院の治験審査委員会(IRB)の承認を受けており、2016年4月28日に医薬品医療機器総合機構(PMDA)に東北大学病院で実施する治験計画届を提出しました。治験期間は2019年8月までを予定しています。
【本治験の実施体制】
治験調整医師:東北大学病院神経内科・教授 青木 正志
治験実施医療機関
① 東北大学病院
治験責任医師:神経内科・教授 青木 正志
② 大阪大学医学部附属病院
治験責任医師:神経内科・脳卒中科・教授 望月 秀樹
【本治験の概要】
本治験では、ALS患者さんの脊髄腔に治験薬を2週間に1回の間隔で繰り返し投与します。治験薬は被験薬「KP-100IT」または「プラセボ」の2種類で、最初の6ヶ月間はそれぞれの参加患者さんにどちらかの治験薬を投与します。これにより、被験薬「KP-100IT」が投与された患者さんと「プラセボ」が投与された患者さんの結果を比較し、被験薬KP-100ITの効果と安全性を評価します。評価に対して主観が入らないよう、それぞれの患者さんに投与された治験薬の種類は患者さんご本人および治験関係者にも知らされない二重盲検下で実施します(二重盲検期)。KP-100ITが投与される確率は2/3、プラセボが投与される確率は1/3です。被験薬「KP-100IT」と「プラセボ」の区別は、すべての患者さんの投与・観察が終了するまで明らかにはされません。
その後、投与の継続を希望される患者さんには全員に被験薬「KP-100IT」を同様に投与し、最長6ヶ月間まで効果と安全性の評価を継続します(継続投与期)。
本治験では、治験薬の脊髄腔内投与のため、専用のカテーテルを脊髄腔に挿入して留置する必要があります。このカテーテルには体内(皮下)に埋め込むポートが付いています。このカテーテルと皮下ポートのセットをNP022と呼びます。本治験に参加していただくALS患者さんは、すべての方にNP022の埋め込み手術を受けていただくことが必要となります。本治験の終了時にはNP022を取り除く手術を行います。
【治験参加期間】
継続投与期に参加される患者さんが最長の6ヶ月まで投与の延長を希望された場合、最初のスクリーニング検査から最後の観察までの期間はおよそ15~16ヶ月です。
この他、本試験に関する情報については、以下のサイトにも掲載しておりますのでご参照ください。
大学病院医療情報ネットワーク臨床試験登録システム(UMIN-CTR):
https://upload.umin.ac.jp/cgi-open-bin/ctr/ctr_view.cgi?recptno=R000025102
【参加基準】
本治験には、以下の「治験に参加できる基準」を満たし、「治験に参加できない基準」に該当しないALS患者さんのみが参加可能です。
「治験に参加できる基準」
以下の条件に該当することが必要です。
<仮登録のための条件>
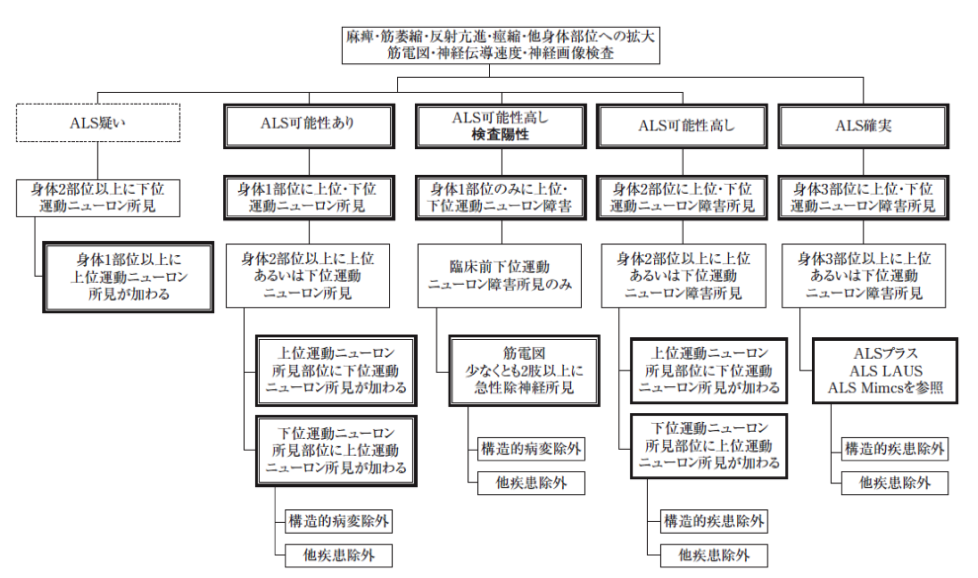
① ALSの診断規準(世界神経学会El Escorial改訂)の 「ALS可能性高し 検査陽性」、「ALS可能性高し」または「ALS確実」に該当し、発症後30ヶ月以内の方
② ALSの重症度分類(厚生労働省 特定疾患研究調査 2007.1.1)が1または2の方
③ 年齢が20歳以上、70歳以下の方
④ ALSFRS-Rの全項目が2点以上の方
⑤ %FVC(呼吸機能)が70%以上の方
⑥ Modified Norris Scale 球症状尺度の全項目が2点以上の方
<本登録のための条件>
仮登録の条件に加えて、以下の条件に合っていることが必要です。
⑦ 前観察期のALSFRS-Rスコアの変化量が -1~-3点の範囲にある方
⑧ カテーテル・ポート埋め込みの前日までに入院し、その後、治験薬の初回投与の翌日まで継続して入院が可能な方
【用語説明】
※1 筋萎縮性側索硬化症 (Amyotrophic Lateral Sclerosis: ALS)
脳や脊髄にある運動神経細胞の障害によって筋萎縮・筋力低下を来たす進行性の疾患で、意識や知覚は保たれたまま手足や体、発音や飲み込み、呼吸といった全身の力が徐々に弱くなってゆく神経疾患。発症すると平均2~5年で呼吸筋麻痺に至ることが多く、発症後3年の生存率は50%に満たないといわれている。患者数は国内で9,000人以上、世界中では35万人。ALSの大部分は原因が明らかとなっていない孤発性ALSだが、全体の5~10%に家族性ALSがあり、近年続々と原因遺伝子が明らかとなっている。ALSの原因として興奮性の神経伝達物質であるグルタミン酸の過剰や酸化ストレスなどいくつかの仮説があるが、発症メカニズムはまだ十分解明されていない。
ALSに対する治療薬は長らくリルゾール(商品名:リルテック)のみであったが、昨年、エダラボン(商品名:ラジカット)が新たに承認された。これらの既存薬はALS進行抑制効果が認められているが不十分なため、より効果の高いALS治療薬の開発が切望されている。
※2 肝細胞増殖因子(Hepatocyte Growth Factor: HGF)
成熟肝細胞の増殖を促進する因子として日本で発見された生理活性タンパク質であるが、その後の研究からHGF は各種上皮系組織や心血管系組織などにも作用することが明らかとなった。HGF は細胞の増殖や組織の再構築を促す活性に加え、細胞死を防ぐ活性や血管新生を促す活性を発揮することによって、外傷や疾病によって障害された組織の再生や保護を支えている。また、脳神経系組織においては、神経栄養因子として神経保護作用や軸索伸展作用を示すことがわかっている。神経栄養因子としてのHGFの作用に基づき、ALSおよび脊髄損傷などの難治性神経疾患に対する治療薬としてのHGFの臨床応用に期待が高まっている。現在、組換えHGFタンパク質を用いて、ALSを対象とする本治験の他にも、脊髄損傷に対する治験が慶應義塾大学のグループを中心に進められている。
【お問い合わせ先】
(ALS患者さんまたはご家族等)
必ず主治医の先生を通してFAXでのお問い合わせをお願いします。
専用FAX番号:
東北大学 022-728-3455
大阪大学 06-6879-3579
専用FAX問い合せ用紙ダウンロード先:
東北大 詳細(神経内科Webサイト) / 問い合わせ用紙ダウンロード
大阪大 詳細(神経内科Webサイト) / 問い合わせ用紙ダウンロード
(その他治験に関すること)
東北大学大学院医学系研究科神経内科学分野
助教 割田 仁 (わりた ひとし)
電話番号:022-717-7189
FAX:022-717-7192
Eメール:warita-ns*umin.net(*を@に変えてください)
(報道担当)
東北大学病院広報室
電話番号:022-717-7149
FAX:022-717-8931
Eメール:pr*hosp.tohoku.ac.jp(*を@に変えてください)
大阪大学医学部附属病院総務課
電話番号:06-6879-5312
FAX:06-6789-5019
Eメール:ibyou-soumu-kouhyo*office.osaka-u.ac.jp(*を@に変えてください)
【参考情報】
A. 筋萎縮性側索硬化症(ALS)の診断基準(世界神経学会El Escorial改訂)
B. 筋萎縮性側索硬化症(ALS)の重症度分類(厚生労働省 特定疾患研究調査 2007.1.1)
1. 家事・就労はおおむね可能
2. 家事・就労は困難だが、日常生活(身の回りのこと)はおおむね自立
3. 自力で食事、排泄、移動のいずれか一つ以上ができず、日常生活に介助を要する
4. 呼吸困難・痰の喀出困難、あるいは嚥下障害がある
5. 気管切開、非経口的栄養摂取(経管栄養、中心静脈栄養など)、人工呼吸器使用
関連資料

 TEL
TEL アクセス
アクセス
 交通アクセス
交通アクセス










